Appunti
- Necessità di capire prima dell’intervento chirurgico la natura di una lesione
- e allo stesso nella diagnostica moderna non è più possibile aspettare l’intervento chirurgico per sapere se una lesione sia benigna o maligna
- la caratterizzazione microistologica di un nodo mammario permette di avere una diagnosi molto vicina a quella istologica definitiva
- Inoltre, la caratterizzazione pre-intervento, permette di impostare un tipo di trattamento più idoneo
- lobulare vs duttale
- in situ vs infiltrante
- una diagnosi di in situ, a meno che nei casi di mastectomia,
- non richiede la biopsia del linfonodo sentinella
- una diagnosi di in situ, a meno che nei casi di mastectomia,
- e allo stesso nella diagnostica moderna non è più possibile aspettare l’intervento chirurgico per sapere se una lesione sia benigna o maligna
- Sul tessuto biopsiato vengono cercati:
- l’assetto recettoriale estrogeni e progesterone (ER, PR)
- HER-2 } suscettibilità a terapie come il trastuzumab
- l’indice di proliferazione (Ki-67)
- l’assetto recettoriale estrogeni e progesterone (ER, PR)
- Se imaging sospetto → biopsia su linfonodo ascellare
- La guida radiologica si usa ogni volta che non ho un corrispettivo come nel caso delle calcificazioni, sia in stereotassi che in tomosintesi;
- la guida RM è molto meno diffusa, almeno in Italia, e si usa qualora, anche a ritroso, i reperti RM non trovano sicura corrispondenza nelle immagini di I livello
- 2nd look ecografico o mammografia con mdc
FNAC
- Prelievo mediante pressione negativa
- risalita delle cellule fino al conetto per aspirazione, una volta che l’ago è centrato nella lesione
- basso costo
- richiede manualità perché l’ago è piccolo
- vengono prelevate solo cellule e non una struttura
- vantaggi
- velocità
- spesso analisi estemporanea
- velocità
- svantaggi
- non posso definire istotipo né infiltrazione
- Importante la concordanza tra il pensiero del radiologo (BI-RADS) ed il ritrovamento dell’anatomopatologo
- se BI-RADS 5 ma C2
- pensare di avere sbagliato il target
- o avere dato poco materiale
- se BI-RADS 5 ma C2
TRU-CUT (CORE BIOPSY)
- Non ho singole cellule ma ho una struttura
- un frustolo con cui fare diagnosi micro-istologica
- tempo fa trovava indicazione quando citologico dubbio
- ormai esame di preferenza
- aghi tra 18 e 14 G, di tipo automatico o semi-automatico
- con il SEMI-AUTOMATICO avanzo l’ago senza tranciare
- in modo da portare la lesione all’interno della camera bioptica sapendo sempre dov’è la punta
- NELL’AUTOMATICO l’avanzamento è simultaneo al prelievo
- va avanti la camera bioptica insieme al tagliente, senza sapere dov’è la punta dell’ago rispetto al tagliente
- l’apertura della camera è importante (22 mm)
- dispositivi che possono fissarla a 10mm oppure 15mm
- con il SEMI-AUTOMATICO avanzo l’ago senza tranciare
- ogni campione prevede che scatti e mi ricentri
- l’ideale per un patologo sarebbero 3-5 frustoli
- possibilità che ci sia un sanguiamento
- anestesia locale con lidocaina
- nella mammella, soprattutto quelle dense e nelle lesioni benigne
- se uso un ago semi-automatico
- c’è la possibilità che la lesione si sposti mentre spingo avanti la camera
- mentre nell’ago automatico questa possibilità è molto meno frequente perché il tagliente viene portato subito avanti con la camera
- stare sempre più paralleli possibili alla parete toracica per evitare il rischio di PNX
- se uso un ago semi-automatico


- B1: tessuto normale inconcluso
- non corrisponde a quanto descritto dal radiologo
- B3: non è come C3 (atipie ma non so cosa sono)
- sono lesioni che rappresentano un rischio di poter trovare li vicino una lesione tumorale
- magari non inclusa dalla biopsia
- categoria di rischio differente di poter sviluppare k mammario
- sono lesioni che rappresentano un rischio di poter trovare li vicino una lesione tumorale
- B5c: c’è una microinvasione
- impossibilità di dire con certezza se la lesione è infiltrante o meno
- B5d quando la lesione è maligna ma non di origine mammaria

- Traumatismo in forse perché più teorico che pratico per i vantaggi che porta
- Il campione deve essere preparato
- non lettura immediata
- Guida stereotassica
- Lo stesso dispositivo può essere impiegato anche con guida stereotassica con ago posizionato in un supporto apposito e infilato sul target mediante coordinate
- La Paziente non è sdraiata (sistemi verticali)
- Nella STX sono sicuramente centrato
- non posso vedere real-time la posizione dell’ago durante lo scatto
- Si seleziona un punto come target
- la macchina imposta le coordinate in maniera automatica sui tre piani dello spazio in base alle caratteristiche dell’ago
- Il detettore funziona in modo che l’immagine sia sempre diagnostica se non sono centrato bene, in modo da centrarmi in maniera ottimale
- L’approccio può essere con paziente
- seduta
- medio-laterale
- latero-mediale
- CC
- in base alla posizione della lesione in modo da fare meno strada possibile con l’ago
- La sedia può diventare un lettino con decubito
- M-L
- L-M
- caudo-craniale
- Esiste anche il tavolo prono con foro dove la mammella entra e si colloca sul detettore
- AGOBIOPSIA VACUUM ASSISTITA (VAB)
- utilizza aghi grossi
- 7-11 Gauge,
- alcuni anche il 12 G sotto guida ecografica
- con un sistema che prevede l'aspirazione forzata
- andando a campionare anche più di 12 frustoli
- rimanendo all’interno della lesione
- con la camera bioptica che ruota di 360° in aspirazione forzata attirando tessuto nella camera stessa
- tessuto che viene poi tagliato e aspirato
- con la camera bioptica che ruota di 360° in aspirazione forzata attirando tessuto nella camera stessa
- rimanendo all’interno della lesione
- utilizza aghi grossi
- Il sistema di aspirazione forzata è utile perché da un lato
- porta via i residui di sangue e i detriti che si creano nel punto di prelievo
- fa si che dentro la camera bioptica ci sia sempre del tessuto evitando l’inconveniente del tru-cut
- per cui, a volte, ripassando con l’ago in un tessuto che è già stato sollecitato
- si ottenga poco tessuto e più sangue
- per cui, a volte, ripassando con l’ago in un tessuto che è già stato sollecitato
- Può essere eseguita con le stesse guide
- US
- stereotassi
- RM
- Non è proposta a tutti perché di solito il tru-cut è più che sufficiente
- ma trova delle INDICAZIONI come
- le PICCOLE MICROCALCIFICAZIONI che sono visibili solo con MX
- piccole e difficilmente intercettabili con ago piccolo
- può risolvere i DUBBI delle lesioni intermedie alla CORE BIOPSY
- addirittura viene proposta l’escissione delle LESIONI B3 con VAB senza ricorrere alla chirurgia
- le PICCOLE MICROCALCIFICAZIONI che sono visibili solo con MX
- ma trova delle INDICAZIONI come
- Il MAMMOTOME usa aghi da 11G
- a differenza dei sistemi odierni
- con esso il frustolo veniva rimosso ogni volta dall’operatore con la pinzetta
- mentre adesso i sistemi sono maggiormente sofisticati
- con esso il frustolo veniva rimosso ogni volta dall’operatore con la pinzetta
- frustoli venivano alloggiati nella parte posteriore come fosse una cartuccera
- poi veniva tolta e veniva scattata la radiografia
- a differenza dei sistemi odierni
- L’ENCORE aspira i frustoli in una gabbietta, che vengono, poi, disposti in un secondo tempo
- Sono sistemi molto automatizzati, in cui noi decidiamo a computer dove e quanto prelevare, quanto aspirare
- se necessario iniettare la lidocaina nel sito di prelievo
- Da notare la punta lanceolata della camera per entrare senza fare un accesso nonostante il grosso calibro
- L’attuale sistema è questo che, in automatico, dispone i frustoli in una gabbia
- ed effettua una radiografia
- in modo da vedere subito se sono presenti le calcificazioni
- ed effettua una radiografia
- GUIDA STEREOTASSICA
- Nella tomosintesi l’asse Z viene stabilito direttamente dalla macchina
- in base a in quale della fetta la lesione risulta a fuoco
- Senza la tomosintesi si usavano principi di trigonometria risultanti dall’acquisizione
- a 90° e a + e – 15°
- c’era un sistema di centratura e in seguito alle acquisizioni la macchina calcolava in automatico la distanza dal detettore
- Infine venivano fatte altre acquisizioni per controllare che l’ago fosse dentro la lesione
- c’era un sistema di centratura e in seguito alle acquisizioni la macchina calcolava in automatico la distanza dal detettore
- a 90° e a + e – 15°
- Il setting viene sempre scelto accuratamente in modo da ottenere la posizione più comoda possibile per evitare movimenti all’esame
- scegliere il percorso più breve possibile per raggiungere la lesione, di solito un tragitto:
- CC per i quadranti superiori
- ML per interni
- LM per esterni
- Nella tomosintesi l’asse Z viene stabilito direttamente dalla macchina
- GUIDA TOMOGRAFICA
- La centratura tomografica garantisce una riduzione della dose valutabile intorno al 30%
- Trova indicazione
- quando lesione non visualizzabile adeguatamente con la MX o con l’US
- La macchina, in automatico, in base alla tipologia di ago che scelgo
- centra la lesione
- mi dice se ho spazio per far entrare l’ago
- se la punta dell’ago andrebbe a finire in spazi pericolosi
- Al termine della procedura viene posizionato un marker di dove ho fatto il prelievo
- se ho aspirato completamente la lesione
- almeno risulta evidenziabile l’area precedentemente campionata
- AGOBIOPSIA RM-GUIDATA
- Il problema principale è che è indicata
- in lesioni non evidenziabili con altre metodiche
- spesso visualizzabili unicamente dopo mdc
- quindi bisogna tenere conto del timing
- La mammella viene posta in una bobina dedicata
- con una griglia per tenerla ferma
- su cui viene posizionato un fiducial che crea un artefatto
- permette di orientare in maniera corretta la griglia ed il posizionamento dell’ago
- su cui viene posizionato un fiducial che crea un artefatto
- con una griglia per tenerla ferma
- Dopo di che si inietta l’mdc
- in modo da evidenziare il box corrispondente alla lesione (assi x e y)
- si posiziona un altro box compartimentato in modo da scegliere la fenestratura più adatta all’inserimento dell’ago
- L’asse z viene calcolato o misurando la distanza dalla cute se acquisiamo in assiale oppure contando la fetta in cui la lesione appare se acquisiamo in sagittale
- E’ una procedura che impegna la macchina 40-45 minuti circa
- per l’inserimento del trocar compatibile con RM
- l’acquisizione di controllo
- una volta che siamo sicuri del posizionamento, si inserisce l’ago effettivo
- facendo uscire il lettino, e si campiona, sempre con sistema VAB
- per essere più confidenti
- facendo uscire il lettino, e si campiona, sempre con sistema VAB
- una volta che siamo sicuri del posizionamento, si inserisce l’ago effettivo
- l’acquisizione di controllo
- per l’inserimento del trocar compatibile con RM
- Dopo di che si posiziona il marker e si fa un’acquisizione di controllo
- I MARKER rilasciati sono visibili praticamente con tutte le metodiche
- creano artefatti in RM
- sono radiopachi
- ecovisibili
- in modo che siamo sicuri che il chirurgo abbia escisso tutto il tessuto necessario
- I MARKER rilasciati sono visibili praticamente con tutte le metodiche
- Il problema principale è che è indicata
- REPERAGE PRE-OPERATORIO
- La chirurgia mammaria è votata alla salvaguardia di quanto più tessuto mammario possibile
- diagnosi più fini possibili
- in modo da evidenziare noduli non palpabili
- che, però, il chirurgo deve trovare in qualche modo
- la strategia più utilizzato è il posizionamento di un repere metallico costituito da un ago ad uncino collegato alla superficie da un sottile filo radiopaco
- verrà poi seguito dal chirurgo, dopo aver verificato che non si sia mosso
- Il reperage in carbone
- prevede l’inserimento dell’ago tramite il quale si colora la regione del nodulo con una soluzione di carbone vegetale e fisiologica
- colorando anche una traccia fino al sottocute in modo che il chirurgo porta via tutto quello che vede di nero
- Può essere messo anche 4-6 mesi prima
- non come il repere metallico che deve essere messo la mattina dell’esame
- La ROLL (Radioguided Occult Lesion Localization)
- maggiormente avanzata ma più costosa,
- prevede l’iniezione un tracciante radioattivo che viene poi evidenziato dal chirurgo con una γ-camera
- un percorso particolare coinvolgente la medicina nucleare
- prevede l’iniezione un tracciante radioattivo che viene poi evidenziato dal chirurgo con una γ-camera
- maggiormente avanzata ma più costosa,
- Ancora più avanzato è il seeding radioattivo
- piccoli semini che possono essere inseriti tempo prima
- ricercabili poi dal chirurgo di nuovo con γ-PET
- piccoli semini che possono essere inseriti tempo prima
- il Magseed e il Localizer sono sistemi avanzati a radiofrequenze
- molto più costosi
- la strategia più utilizzato è il posizionamento di un repere metallico costituito da un ago ad uncino collegato alla superficie da un sottile filo radiopaco
- che, però, il chirurgo deve trovare in qualche modo
- in modo da evidenziare noduli non palpabili
- diagnosi più fini possibili
- La chirurgia mammaria è votata alla salvaguardia di quanto più tessuto mammario possibile
- In corso di intervento chirurgico indispensabile la verifica radiologia
- non viene fatto un esame estemporaneo
- ma viene effettuata una radiografia o in sala operatoria o radiografica
- confrontando il pezzo con le immagini mammografiche in modo che il radiologo possa dire se la lesione è stata presa o meno
- e, se confidente, qual è il margine,
- in modo che eventualmente il chirurgo vada ad allargarlo
- e, se confidente, qual è il margine,
- confrontando il pezzo con le immagini mammografiche in modo che il radiologo possa dire se la lesione è stata presa o meno
- ma viene effettuata una radiografia o in sala operatoria o radiografica
- non viene fatto un esame estemporaneo
- PROCEDURE PERCUTANEE
- Inizialmente non hanno riscontrato molto successo
- poiché nel momento in cui la chirurgia è controindicata per le comorbilità
- l’oncologo preferiva impostare l’ormonoterapia (se K sensibile)
- l’ormonoterapia prolungata, però, espone le Pazienti anziane, a complicanze come l’osteoporosi
- l’oncologo preferiva impostare l’ormonoterapia (se K sensibile)
- poiché nel momento in cui la chirurgia è controindicata per le comorbilità
- Breast lesion excision system (BLES)
- Radiofrequenze (RF)
- Crioablazione
- High intensity focused ultrasound (HIFU)
- stando attenti alla vicinanza della lesione con la cute o la fascia e che abbia una dimensione accettabile a questi trattamenti;
- al momento rimangono alternative in casi selezionati
- Inizialmente non hanno riscontrato molto successo
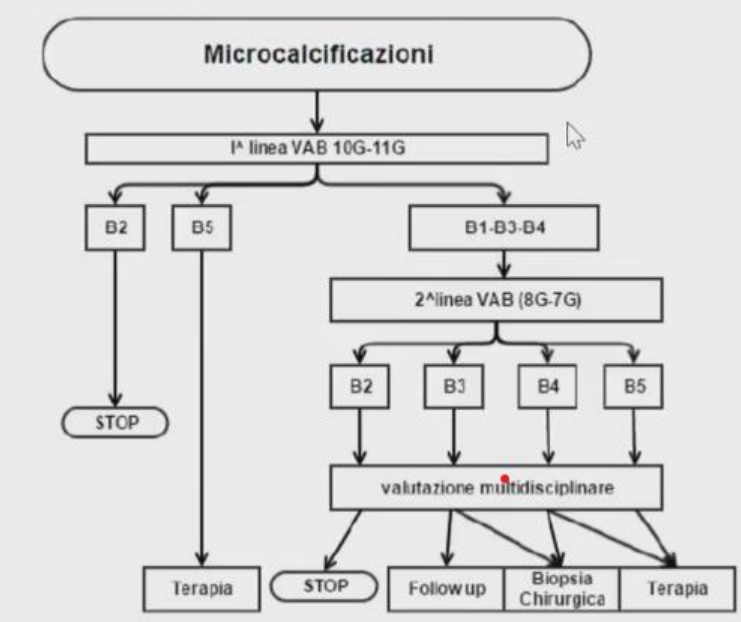
- MICROCALCIFICAZIONI
- derivano dal deposito di ossalato di calcio e fosfato di calcio nel tessuto mammario
- se le troviamo lungo le pareti dei vasi non le tocchiamo
- ma constatiamo il rischio cardiovascolare della Paziente
- se sono disposte lungo il dotto o hanno determinate caratteristiche
- dobbiamo verificare se sono benigne o maligne
- Sono un punto cruciale nella senologia
- possono essere tutto e nulla
- se non diagnosticate da segno che erano di lesione in situ possiamo trovare
- una lesione infiltrante
- oppure la lesione può rimanere in situ ma aumentare di estensione
- andando a cambiare la gestione della Paziente
- se non diagnosticate da segno che erano di lesione in situ possiamo trovare
- possono essere tutto e nulla
- L’OSSALATO DI CALCIO si associa più spesso a BENIGNITÀ
- si trova nelle MODIFICAZIONI FIBROCISTICHE
- anche se possono associarsi anche a lesioni maligne
- si trova nelle MODIFICAZIONI FIBROCISTICHE
- Il FOSFATO DI CALCIO molto più spesso si trova nelle LESIONI MALIGNE
- Il radiologo deve valutare
- morfologia
- distribuzione
- quantità
- sui piccoli gruppi non è facile fare distinzione
- sarà necessario proseguire con campionamento
- Il radiologo deve valutare
- la CITOLOGIA non è oggigiorno neanche proponibile
- il TRU-CUT ha forti limitazioni dal momento in cui si tratta di aree piccole con ago che entra ed esce
- solo con la core biopsy rischio di sottostimare le lesioni con calcificazioni del 17-32%
- e con il tessuto che può sanguinare o mobilizzarsi con il movimento dell’ago
- spesso richiedono guida mammografica o stereotassica
- in quanto evidenziabili solo con questa metodica
- 1 su 3 casi possono essere inadeguati o portare ad un campionamento insufficiente per una diagnosi corretta,
- 1 su 3 casi possono essere inadeguati o portare ad un campionamento insufficiente per una diagnosi corretta,
- in quanto evidenziabili solo con questa metodica
- spesso richiedono guida mammografica o stereotassica
- e con il tessuto che può sanguinare o mobilizzarsi con il movimento dell’ago
- solo con la core biopsy rischio di sottostimare le lesioni con calcificazioni del 17-32%
- VAB permette una maggior qualità dei frustoli
- comporta un maggior lavoro per l’anatomopatologo
- con tempi di refertazione più lunghi
- centratura in tomosintesi può essere utile per centrare il target in maniera più corretta:
- capitava che nelle calcificazioni più sparse
- con la stereotassi uno non centrasse il target in maniera corretta sulle due proiezioni
- si può usare la vab anche con guida us e in questo caso è fondamentale fare la radiografia del prelievo per essere sicuri
- Con la VAB il rischio di sottostima si riduce molto (11% circa)
- Le complicazioni (dolore e sanguinamento) da letteratura sono più frequenti (3% circa vs 0.4%)
- comunque i vantaggi sono maggiori perché posso non essere diagnostico e ripetere il campionamento
- capitava che nelle calcificazioni più sparse
- comporta un maggior lavoro per l’anatomopatologo
Raccolta di immagini
Non sono state rilevate immagini associate all'espressione
"Interventistica senologica"
puoi provare a cercare con un'altra parola chiave oppure consultare l'Atlante di Radnote
puoi provare a cercare con un'altra parola chiave oppure consultare l'Atlante di Radnote